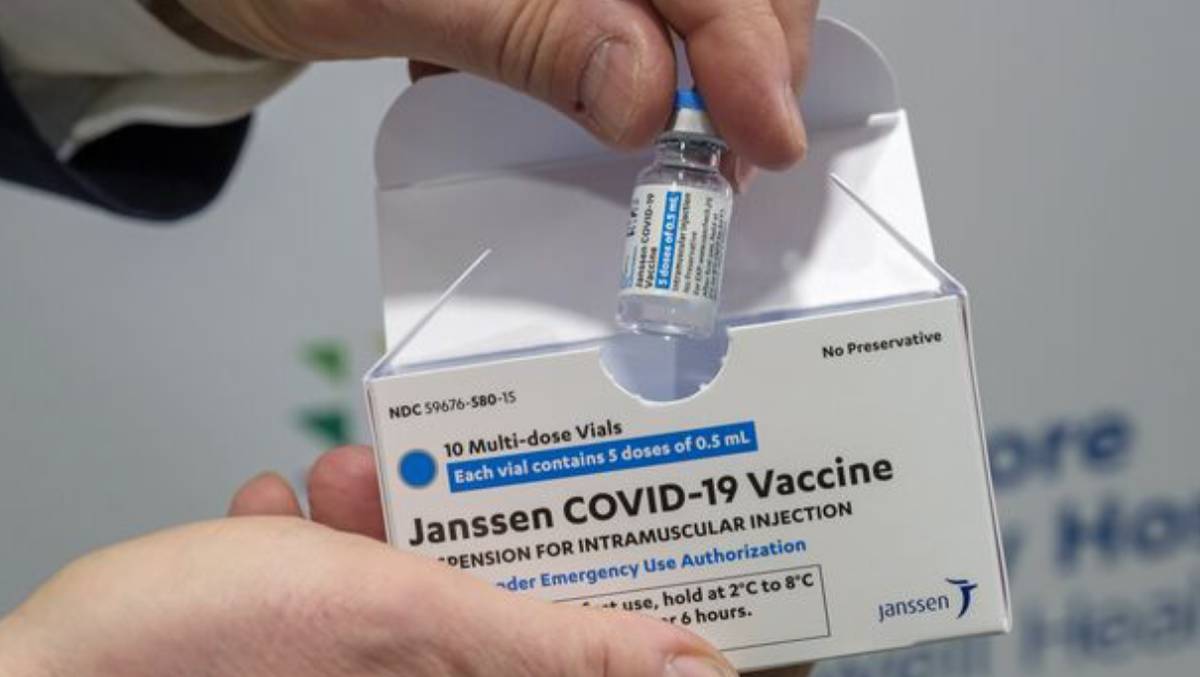
Il vaccino Johnson & Johnson arriva anche in Italia. Via libera dunque al siero anti-Covid monodose prodotto dalla Janssen, sussidiaria della multinazionale americana. Sarà destinato in via prioritaria agli over 60 secondo le indicazioni di Aifa, l’Agenzia italiana del farmaco. Come funziona il vaccino Johnson & Johnson? Ecco tutto quello che sappiamo su questo nuovo siero che contribuirà a far accelerare la campagna vaccinale in Italia. (continua a leggere dopo la foto)

Vaccino Johnson & Johnson Italia: la storia del siero prodotto dalla sussidiaria Janssen
Il 29 gennaio 2021, Janssen, la sussidiaria produttrice di vaccini del gigante farmaceutico Johnson & Johnson, ha annunciato i dati della sua sperimentazione clinica di fase 3 per il suo vaccino Covid-19. La sperimentazione ha monitorato i partecipanti dopo che avevano ricevuto solo una dose del suo vaccino, un vantaggio potenzialmente considerevole rispetto agli altri sieri finora disponibili.
Tutti gli altri vaccini disponibili o in fase avanzata di sperimentazione clinica richiedono infatti due dosi, il che complica la logistica della distribuzione. Inoltre, il siero anti Covid di Janssen richiede solo una refrigerazione regolare (quindi l’utilizzo di normali celle frigorifere) per essere spedito e conservato. Insieme, questi due fattori potrebbero rendere significativamente più facile inoculare rapidamente vaste aree della popolazione globale. Ecco cosa sappiamo, e non sappiamo, del vaccino finora.
Come funziona il vaccino per il Covid-19 Janssen Johnson & Johnson
Il vaccino Janssen è un vaccino vettore virale. Ciò significa che utilizza un virus – in questo caso, una versione di un adenovirus, che causa lievi sintomi di raffreddore o influenza nelle persone. L’azienda ha modificato questo virus per includere il DNA che codifica per la proteina spike sul virus SARS-CoV-2. Questa proteina spike è una delle caratteristiche di identificazione del virus per le cellule immunitarie e ciò che il virus usa per farsi strada nelle nostre cellule.
L’adenovirus si insinua nelle nostre cellule come farebbe normalmente un virus, ma poi inietta il materiale genetico per la proteina spike. Le nostre cellule fanno quello che sanno fare meglio e leggono quel DNA per creare copie della proteina spike, che poi innescano una reazione immunitaria. Questa funzione è simile a un vaccino a mRNA , tranne per il fatto che il processo di produzione della proteina spike inizia nel DNA rispetto allo stadio mRNA nella traduzione della proteina.
È simile al vaccino Covid-19 di AstraZeneca, che utilizza anche un adenovirus di scimpanzé per trasportare il DNA che codifica per la proteina spike SARS-CoV-2. Tuttavia, quel vaccino è stato testato solo con due dosi e la FDA non ha ancora concesso l’autorizzazione per l’uso di emergenza. Janssen ha un vaccino simile per l’Ebola, che la FDA ha approvato alla fine del 2019. Le autorità di regolamentazione europee lo hanno approvato nel luglio 2020.
Vaccino Johnson & Johnson Italia: i risultati della sperimentazione
La sperimentazione del vaccino anti Covid Janssen Johnson & Johnson è stata svolta su una platea di 43.783 partecipanti negli Stati Uniti, America Latina e Sud Africa. Secondo i dati comunicati dall’azienda, il vaccino ha prevenuto circa il 66% dei casi di Covid-19 . La società ha trovato prove di una certa immunità nei partecipanti due settimane dopo aver ricevuto l’iniezione, immunità che sembrava rafforzarsi nel tempo. Ha anche protetto contro l’85% dei casi di Covid-19 da moderati a gravi – i casi da ricovero insomma – e finora ha presentato una protezione completa dalla morte per Covid-19.
Tuttavia, questi risultati variavano a seconda di dove si trovavano i partecipanti allo studio. Negli Stati Uniti, il vaccino ha prevenuto il 72% dei casi di Covid un mese dopo; in Sud Africa, era solo il 57%. In America Latina, era del 66%. Questi diversi tassi di efficacia sono il risultato dei diversi ceppi di SARS-CoV-2 presenti in questi diversi paesi, le ormai famose varianti. In Sud Africa, la variante predominante, chiamata B.1.351, costituiva la maggior parte dei casi di Covid-19 nello studio, il che suggerisce che il vaccino ha una minore efficacia su di essa.
Per quanto riguarda la platea su cui si è svolta la sperimentazione, un terzo dei partecipanti aveva 60 anni o più. Due terzi di loro erano bianchi, il 45% erano ispanici di latino e circa il 20% erano neri. Meno del 10% erano nativi americani e solo il 3% erano asiatici.
La sospensione negli Usa e il via libera di Ema il 20 aprile 2021
Come detto, lo scorso 13 aprile la Fda, Food and Drugs Administration americana, ha bloccato in via cautelativa il siero Johnson & Johnson. Il motivo alcune reazioni avverse, con episodi di trombosi. “Quello che vediamo per i vaccini Johnson & Johnson è simile a quanto osservato con AstraZeneca”, avevano affermato le autorità sanitarie americane. E’ bene precisare che per quanto riguarda gli Usa si è trattato di soli 6 casi su circa 7 milioni di somministrazioni complessive del siero, uno con esiti fatali.
L’Agenzia europea del farmaco (Ema), dopo la revisione della documentazione clinica disponibile, lunedì 20 aprile 2021 ha dato il suo via libera alla somministrazione del vaccino Janssen Johnson & Johnson. La revisione dell’ente regolatorio europeo ha riconosciuto “possibili” legami di causa-effetto tra il vaccino di Johnson & Johnson e gli eventi “molto rari” di trombosi cerebrale che si sono verificati negli Usa. Lo si legge in una nota dell’agenzia Ue nella quale si precisa però che “i benefici superano i rischi”. Le indagini di Ema sul siero, in ogni caso, proseguono.
